Experiencia con insulina degludec en pacientes diabéticos Tipo 1 del Hospital San Juan de Dios
Santiago
Lilian Sanhueza M.1,3, Pilar Durruty A.1,2,a, Guillermo Santibáñez G.1,b, Elizabeth Toro T.1,c, Juan Pablo Miranda O.2 y Manuel García de los Ríos A.1
Experience with degludec Insulin in Type 1 diabetic patients at the San Juan de Dios Hospital
1Unidad de Diabetes, Hospital San Juan de Dios, Servicio y Departamento de Medicina Occidente. Profesor Asociado de la Universidad de Santiago de Chile.
2Servicio de Endocrinología y Diabetes, Hospital Clínico Universidad de Chile.
3Facultad de Ciencias Médicas, Universidad de Santiago de Chile.
aBioquímico.
bPsicólogo.
cEnfermera
Correspondencia:
Lilian Sanhueza
Fray Camilo Henríquez 175
Depto. 404 Santiago.
ilianllay@yahoo.es
Recibido: 05-06-2017
Aceptado: 04-08-2017
Objective: To study the efficacy and safety of degludec insulin in Type 1 diabetic patients. Patients and Method: In a prospective study, 230 type 1 diabetics patients, average aged 34 years age and 14 years of diagnosis of diabetes and treated with two doses of insulin glargine U-100, were changed to degludec. Patients had glycosylated hemoglobins (HbA1c) greater than 10%. Results were recorded at 3 and 6 months with parameters clinical, biochemical, insulin requirements per kilogram of weight (U/kg/wt) and hypoglycemia. Capillary glycemia was evaluated three times a day and the dose of insulin degludec every two weeks. The statistical analysis used was average and rank, standard deviation, normal Swilk test, categorical Chi2 and continuous ANOVA or Kwallis, and p < 0.05. A psychological survey was conducted to evaluate satisfaction with the new treatment. Results: Fasting blood glucose decreased from 253 (range 243-270) at 180 mg/dl (172-240) at 3 months and at 156 (137-180) at 6 months after the change insulin (p < 0.05). HbA1c, initially 10.6% (10.4-12.2) decreased to 8.7% (9.3-10.1) and 8.3% (8.7-9.7) at 3 and 6 months, respectively (p < 0.05). There was a decrease in basal insulin requirements from 0.7 to 0.4 U/kg/60% reduction in hypoglycaemia; both mild and moderate and severe. Isolated nocturnal hypoglycaemias were recorded in only 4 patients in this group. Conclusion: Six months of treatment with degludec insulin reduces fasting blood glucose, glycosylated hemoglobin and hypoglycemia, both mild and moderate severe and nocturnal, which makes this new ultra-long acting basal insulin a safe and effective tool for the management of type 1 diabetics patients.
Key words: Glargine insulin, deglude insulin, Type 1 diabetes.
Introducción
Desde el descubrimiento y posterior uso clínico de la insulina en 1921, la industria farmacéutica ha desarrollado diferentes tipos de insulinas.
En los últimos diez años aparecen los análogos de insulina por modificaciones en la estructura química de la hormona, obteniéndose insulinas de acción ultrarrápida y ultralenta; a objeto de mantener un control más estable de las glicemias y replicando la secreción fisiológica de la hormona1,2. Las primeras insulinas basales glargina y detemir superiores a la NPH, no cubren en su actividad las 24 h y en muchos casos deben emplearse en dosis fraccionadas cada 12 h2.
Los cambios realizados a la insulina humana son: remoción del aminoácido treonina en posición B30 y adición de un ácido graso de 16 carbonos unido al aminoácido lisina en posición B29 por medio del ácido glutámico. Esta modificación confiere a la insulina degludec propiedades que le permiten formar un depósito soluble de multihexámeros tras su administración subcutánea. Se produce una liberación paulatina de iones de zinc y disociación gradual de los monómeros de insulina, que pasan a la circulación de forma lenta y sostenida4. Su perfil farmacocinético es plano y estable, su vida media es de aproximadamente 25 h y su variabilidad glicémica reducida con respecto a glargina U-1005-7. Una completa revisión respecto a insulina degludec es la realizada por Cahn et al. en el 20158; quienes confirman por los ensayos clínicos disponibles, los beneficios de degludec frente a los demás análogos de insulina en el tratamiento de la diabetes tipo 2 (DM2). Yamamoto et al.9, confirmaron recientemente los hallazgos de otros autores en DM1 tratados con degludec. Birkeland et al.10 en un estudio multicéntrico comparó la eficacia y seguridad de degludec vs glargina en DM1, con una inyección diaria y el agregado de insulina aspártica ultrarrápida en bolos precomidas. Los autores concluyen que la insulina degludec tiene una eficacia similar a la glargina, pero con menor frecuencia de hipoglicemias. Es sabido que cuanto más estricto es el control glicémico, mayor es la frecuencia de hipoglicemias, tanto para diabéticos tipo 1 (DM1) como DM2.
A igual conclusión llegaron Dzygalo et al., agregando que el uso de degludec se asoció, además, a menores requerimientos de insulina11.
Desde hace un año (2016) el comité de farmacia del Hospital San Juan de Dios, aprobó la incorporación de degludec a nuestro arsenal terapéutico.
Pacientes y Método
Participaron 230 DM1, 120 hombres y 110 mujeres, edad promedio 34 años (rango 15-58), antigüedad de la diabetes 14 años (rango 3-46), en control en la Unidad de Diabetes del Hospital San Juan de Dios, Santiago.
Todos los pacientes estaban en tratamiento con glargina (U-100) en dos dosis al día como insulina basal, y ultrarrápida precomidas, a dosis fija, y ajustes de acuerdo a los requerimientos preestablecidos de cada paciente y el conteo de carbohidratos. Todos ellos con HbA1c superiores a 10%. Del total de pacientes cambiados a degludec, algunos presentaban comorbilidades tales como cardiopatía coronaria un 30%, nefropatía diabética un 35%, hipertrigliceridemia 53% e hipertensión arterial un 45%.
La insulina glargina se cambió por degludec iniciándose esta última con 0,3 U/kg/peso y ajustes quincenales según los registros individuales de tres glicemias capilares al día realizados por los propios pacientes; en horario de ayunas, prealmuerzo y precena. La degludec se inyectó en una dosis diaria matinal respetando un horario fijo. La insulina ultrarrápida se mantuvo igual. Los controles por enfermería se realizaron cada 15 días y el control de nutrición mensualmente.
Los pacientes fueron evaluados al inicio, a los 3 y 6 meses de iniciada degludec, considerándose los siguientes parámetros: índice de masa corporal (IMC kg/m2), presión arterial sistólica y diastólica (mm Hg), colesterol total (mg/dl), colesterol HDL (mg/dl), colesterol LDL (mg/dl), triglicéridos (mg/dl), creatinina (mg/dl) y las variaciones en las dosis de insulina (U/kg/peso). Las glicemias, el col-HDL y los TG se midieron con métodos enzimáticos colorimétricos en un equipo automatizado Architec 8.000, con coeficientes de variación (CV) < 5%. Para las glicemias se usó hexoquinasa/6, para el col-HDL y TG un detergente acelerador selectivo. Las HbA1c se determinaron en columnas de cromatografía líquida de alta resolución (HPLC) con un CV < 5%, utilizando un equipo HPLC Variant 2000. La presión arterial se midió en dos oportunidades con un esfingomanómetro de Hg, estando los pacientes sentados en dos repeticiones y sin haber fumado ni recibido alimentos recientemente. El peso y la talla se midieron en una balanza marca Seca con cartabon. Se calculó el IMC expresado como kg/m2.
Respecto a las hipoglicemias (glicemia capilar < 70 mg/dl) se registraron los episodios diurnos y nocturnos y el grado de severidad calificado como leve, moderado y grave. Se consideró hipoglicemia leve aquella que no tenía compromiso neurológico y era manejada por el propio paciente; moderada cuando presentaba alteración de conciencia, pero la persona tenía un estado de alerta suficiente como para tratarla por sí mismo, y grave cuando necesitó la atención de terceros.
En este estudio se aplicó una encuesta psicológica denominada “Escala de satisfacción con el tratamiento recibido”, utilizada para evaluar el impacto del tratamiento en la salud mental de los individuos, en este caso, con el nuevo tipo de insulina. Se utilizó la escala de Feixas et al.12 adaptada por el psicólogo clínico de la unidad y que consiste en cuatro preguntas, cada una con una calificación de 0 a 4 y que los pacientes debieron responder al final del tratamiento. El grado de satisfacción se mide con la pregunta A. La B, permite conocer la percepción de mejoría. La pregunta C evalúa el estado emocional cuando empezó la terapia y la D al finalizarla (Tabla 1).
Tabla 1. Escala de satisfacción con el tratamiento recibido
A. En general ¿Qué tan satisfecho (a) está con su nuevo tratamiento
de insulina? |
B. ¿En qué medida le ha ayudado el nuevo tratamiento con su
control de las glicemias? |
C. ¿Cuál era su estado emocional general cuando empezó el
nuevo tratamiento? |
D. ¿Cuál es su estado emocional general en este momento? |
Las variables clínicas, antropométricas y de laboratorio se expresaron como promedio y rango. A los pacientes se les citó cada 15 días para revisión de glicemias capilares y vigilancia de eventuales hipoglicemias, con reeducación constante en el manejo de estas.
En el análisis estadístico, se utilizó promedio y rango, se evaluó la normalidad de las variables con el test Swilk; para las categóricas se utilizó χ² o Fisher y para continuas se empleó ANOVA o Kwallis, según correspondía. Se realizó análisis en Stata 12.0, considerándose estadísticamente significativo un valor de p < 0,05.
Resultados
Los pacientes presentaron una disminución significativa de la glicemia de ayunas, de 253 (rango 243-270) mg/dl al inicio del tratamiento, a los 3 meses de 180 (172-240) (p < 0,05) y a los 6 meses de 156 (137-180) (p < 0,05). Cabe mencionar que durante los primeros 10 días, la glicemia no desciende, más bien se eleva, probablemente secundario al aumento de los anticuerpos antiinsulina. Es recomendable advertir de esta situación al paciente. En relación a los niveles de HbA1c se observó un comportamiento similar; el valor basal estando con insulina glargina fue de 10,6% (rango 10,3-12,2), a los tres meses bajó a 8,7% (8,2-11,1) y a 8,3% (8,0-9,6) a los seis meses, ambas estadísticamente significativas respecto a la basal (p < 0,05). En la Tabla 2 se presentan las características antropométricas, clínicas y metabólicas de los 230 pacientes DM1. Se aprecia que no hubo cambios importantes en el IMC en toda la observación a pesar de ser estadísticamente significativo (p < 0,05), como tampoco modificaciones significativas en el colesterol total, colesterol HDL, colesterol LDL y creatinina. Los triglicéridos, si bien bajaron en promedio de 182 a 151 mg/dl, no alcanzaron significancia estadística. La dosis de insulina glargina que se administraba a los pacientes antes de cambiar a degludec era de 0,7 U/kg/peso (rango 0,6-0,8). El tratamiento con insulina degludec se inició con 0,3 U/kg/peso, se mantuvo a los tres meses y a los seis meses subió a 0,4 U/kg/peso (0,3-0,5).
La dosis de insulina ultrarrápida se mantuvo igual; solo en 3 casos no hubo necesidad de seguir inyectándola. No se registraron modificaciones en la presión arterial. Las pruebas hepáticas se mantuvieron en rangos normales. No hubo manifestaciones de lipodistrofia ni alergia en el sitio de punción.
En relación a las hipoglicemias, durante los tres primeros meses de tratamiento, se registraron en cada paciente un promedio mensual de 19 hipoglicemias: 14 leves, 4 moderadas y una grave, a los seis meses se presentaron 8 leves y 2 moderadas. Se registraron hipoglicemias nocturnas solo en 4 pacientes de este grupo (Figura 1).
Respecto a la encuesta de satisfacción con insulina degludec, el 84% expresó una alta satisfacción y el 94% manifestó una percepción de mejoría (Figura 2).
Tabla 2. Características antropométricas, clínicas y metabólicas de 230 pacientes DM1 al inicio, a los 3 y 6 meses de seguimiento expresadas como promedio y rango
| Basal | 3 meses | 6 meses | p | |
IMC (kg/m2) |
24 (23-26) |
25 (24-26) |
24 (22-26) |
p < 0,05 |
HbA1c (%) |
10,6 (10,3-12,2) |
8,7 (8,2-11,1) |
8,3 (8,0-9,6) |
p < 0,05 |
Glicemia de ayunas (mg/dl) |
253 (243-270) |
180 (172-240) |
156 (137-180) |
p < 0,05 |
Dosis de insulina (U/kg/peso) |
0,3 |
0,3 |
0,4 |
(-) |
P. A sistólica (mmHg) |
123 (112-144) |
130 (113-145) |
127 (110-150) |
NS |
P. A. diastólica (mm Hg) |
63 (60-75) |
68 (63-80) |
60 (57-70) |
NS |
Colesterol total (mg/dl) |
192 (179-206) |
186 (177-196) |
193 (182-205) |
NS |
Colesterol HDL (mg/dl) |
53 (46-61) |
51 (45-57) |
53 (47-59) |
NS |
Colesterol LDL (mg/dl) |
113 (99-126) |
111 (98-123) |
116 (102-129) |
NS |
Triglicéridos (mg/dl) |
182 (104-259) |
184 (132-237) |
151 (115-186) |
NS |
Creatinina (mg/dl) |
0,8 (0,7-1,8) |
0,8 (0,6-1,8) |
NS |
|
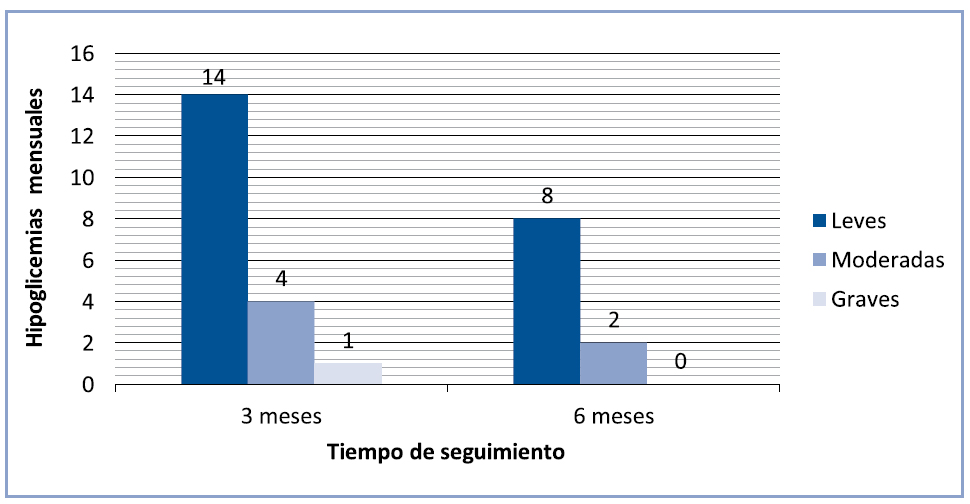 Figura 1. Episodios de hipoglicemia con insulina degludec a los 3 y 6 meses de tratamiento.
Figura 1. Episodios de hipoglicemia con insulina degludec a los 3 y 6 meses de tratamiento.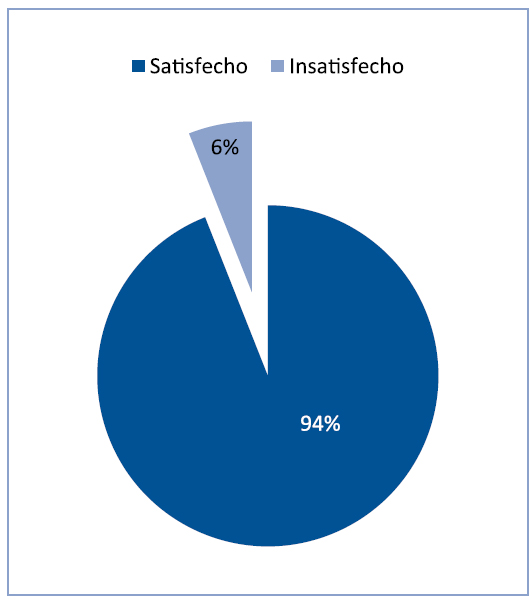 Figura 2. Percepción de mejoría del nuevo tratamiento
Figura 2. Percepción de mejoría del nuevo tratamientoDiscusión
El análisis de los resultados a los 6 meses de iniciada la insulina degludec, es un período de observación muy corto para ser concluyente acerca de los resultados. Además, tiene la desventaja de carecer de grupo control. No se descarta la posibilidad de sesgo en los resultados por la vigilancia y seguimiento muy estrecho de los pacientes. El estudio BEGIN13, que tuvo 52 semanas de duración, demostró que degludec no era superior a la glargina en la reducción de las glicemias de ayunas ni en la HbA1c. En nuestra experiencia hubo reducción de la glicemia de ayunas y HbA1c, a los tres meses de iniciada degludec; sin embargo, a los 6 meses la reducción no es tan significativa. Birkeland et al. no concuerdan con nuestros hallazgos10. No se realizó examen de monitoreo continuo de glucosa lo que habría aportado mayor objetividad a los resultados. Tampoco se midieron los niveles de anticuerpos antiinsulina y no hubo reducción de peso, a pesar de la disminución de la dosis de insulina. Las edades de los pacientes fluctuaban en un rango muy amplio de 18 a 58 años, con motivaciones y situaciones metabólicas distintas, hecho que pudiese haber influido en los resultados.
Sin embargo, cabe destacar el importante grupo de pacientes tratados en esta experiencia que replica los resultados de estudios internacionales14.
Se contó con apoyo psicológico y de enfermería, lográndose una mayor estabilidad emocional que se tradujo en una mejoría del control glicémico. Estos resultados son concordantes con lo informado por otros autores15,16, quienes encuentran una mejor calidad de vida medida como salud mental y función social en los pacientes que usaron insulina degludec.
En nuestro análisis se observó una reducción de 30% la dosis de insulina a los 6 meses. Estos resultados son apoyados por Nakae et al14, quienes encontraron que la dosis de insulina disminuyó de 0,71 U/kg/peso a 0,67 U/kg/peso (p < 0,02) a los seis meses de iniciada degludec. Dzygalo et al.11 en un metaanálisis también confirma la reducción de dosis de insulina comparado con otros análogos de acción lenta. Yamamoto9 refiere que la dosis de insulina al usar degludec se redujo en un 25%, pero que la variabilidad glicémica en 24 h no fue diferente a glargina; el autor concluye que las dos dosis de esta insulina pueden ser reemplazadas por una inyección diaria de degludec. Estos hallazgos concuerdan plenamente con lo publicado por casi todos los autores10,11,15-17. Sólo Nakae14 informa que no hubo diferencias en cuanto a frecuencia y severidad de hipoglicemias con degludec comparado con glargina en las 24 semanas de observación, sugiriendo que con este nuevo análogo se deben usar menores dosis de insulina, tal como fueron nuestros propios resultados.
Gold et al.16 planteó que los episodios severos de hipoglicemia son menos frecuentes en los pacientes en estado alerta y que, aquellos que están en riesgo de estos eventos se debería a una falta de glucagón y a una respuesta reducida de las hormonas de contrarregulación. El trabajo publicado por Koehler et al17, quienes en 38 DM1 randomizados a degludec o glargina estudiaron la respuesta fisiológica aguda frente a una hipoglicemia inducida por estas insulinas, no registró diferencias en los síntomas ni en la función cognitiva; sin embargo, los pacientes con degludec tenían niveles moderadamente superiores de hormona de crecimiento, cortisol, adrenalina y noradrenalina, pero similares en glucagón; frente a iguales tiempos de recuperación de las glicemias plasmáticas.
En otros estudios sobre el uso clínico de degludec18-20 los autores concluyen que esta insulina minimiza el riesgo de hipoglicemias nocturnas como fuera comprobado en nuestra experiencia.
Referencias bibliográficas
- Rhodes C, Shoelzon S, Halban P. 2007. Biosíntesis, procesamiento y química de la insulina. En: Kahn CR, King G, Moses A, Weir G, Jacobson A, Smith R. Joslin´s Diabetes Mellitus 14th ed. Barcelona: Editorial WoltersKluwer; 65-84.
- Durruty P, Pérez-Bravo F. 2014. Patogénesis de la Diabetes Mellitus. En: García de los Ríos M, Durruty P. Diabetes Mellitus 3era ed. Santiago, Chile. Editorial Mediterráneo; 25-39.
- Rosenstock J, Dailey G, Massi-Benedetti M, Fritsche A,
Lin Z, Salzman A. 2005. Reduced hypoglycemia risk with
insulin glargine. A meta-analysis comparing insulin glargine
with human NPH insulin in type 2 diabetes. Diabetes Care 28: 950-955. - Haak T, Tiengo A, Draeger E, Suntum M, Walhaust W. 2005. Lower within-subject variability of fasting blood glucose and reduced weigth gain with insulin detemir compared to NPH
insulin in patient with type 2 diabetes. Diabetes Obes Metab 7: 56-64. - Jonassen I, Havelund S, Hoeg-Jensen T, Steensgaard DB, Wahlund DO, Ribel U. 2012. Design of the novel protraction mechanism of insulin Degludec, an ultra-long-acting basal insulin. Pharm Res 29: 2104-2114.
- Jonassen I, Havelund S, Ribel H, Hoeg-Jensen T, Steensgard DB, Johansen T, et al. 2010. Insulin degludec is a new generation ultra-long acting basal insulin with a unique mechanism of protraccion base on multi-hexamer formation (Abstract) Diabetes 59 (Suppl 1): A11.
- Simó R. 2013. Nueva insulina basal de acción ultralenta: insulin degludec. Av Diabetol 29 (1): 4-11.
- Cahn A, Miccoli R, Dardano A, Del Prato S. 2015. New forms of insulin and insulin therapies for the treatmen of type 2 diabetes. Lancet Diabetes Endocrinol 3: 638-642.
- Yamamoto Ch, Miyoshi H, Fujiwara Y, Kameda R, Ichillama M, Nomoto H, et al. 2016. Degludec is superior to glargine in terms of daily glycemic variability in people with type 1 diabetes mellitus. Endocrine Journal 63: 53-60.
- Birkeland KI, Home PD, Wendisch U, Ratner KE, Johansen T, Endahl L, et al. 2011. A randomized control trial of a new-generation ultralongacting insulin compared with insulin glargine. Diabetes Care 34: 661-665.
- Dzygalo K, Gollicky D, Kowalska A, Szypowska A. 2015. The beneficial effect of insulin degludec on nocturnal hypoglycaemia and insulin dose in type 1 diabetic patients: a systematic review and meta-analysis of randomised trials. Acta Diabetol 52: 231-238.
- Feixas G, Pucurrul D, Roca C, Paz C, García-Grau E, Bados A. 2012. Escala de Satisfacción con el Tratamiento Recibido (Cres-4). Revista de Psicoterapia 23: 52.
- Heller S, Buse J, Fisher M, Garg S, Marre M, Merker L, et al. 2012. Insulin degludec, an ultra-long-acting basal insulin, versus insulin glargine in basal-bolus treatment with meal time insulin aspart in type 1 diabetes (BEGIN Basal BolusType 1: A phase 3, randomised, open-label, treat to target, non inferiority trial. Lancet 2012; 379: 1489-1497.
- Nakae R, Kusunoki Y, Katsuno T, Tokuda M, Akagami T, Murai K, et al. 2014. Medium-Term Effects of Insulin degludec on Patients with Type 1 Diabetes Mellitus. Drugs 14: 133-138.
- Ratner RE, Gough SCL, Mathien C, Del Prato S, Bode B, Mercebach H, et al. 2013. Hypoglycemia risk with insulin degludec compared with insulin glargine in type 2 and type 1 diabetes: a pre-planned meta-analysis of phase 3 trials. Diabetes Obesity and Metabolism 15: 175-184.
- Gold AE, MacLeod KM, Frier BM. 1994. Frecuency of severe hypoglycemia in patients with type 1 diabetes with impaired awareness of hypoglycemia. Diabetes Care 17: 697-703.
- Koehler G, Heller S, Korsatko S, Roepstorff C, Rasmussen S, Haahr H, et al. 2014. Insulin degludec is not associated with a delayed or diminished response hypoglycaemia compared with insulin glargine in type 1 diabetes: a double-blind randomized crossover study. Diabetologia 47: 40-49.
- Muñoz M. 2014. Degludec, una nueva insulina basal de acción ultralenta para el tratamiento de la diabetes tipo 1 y 2: avances en investigación clínica. Endocrinol Nutr 61 (3): 153-159.
- Home PD Meneghini L, Wendish U, Ratner RE, Johansen T, Christensen TE, et al. 2009. Improved health status with insulin degludec compared with insulin glargine in Woodward A, Weston P, Casson IF, Gil GV. Nocturnal hypoglycaemia in type 1 diabetes-frecuency and predictive factors. QJM 102: 603-607.
- Kalra S, Barvah MP, Nizzi AR. 2012. Degludec: A Novel Basal Insulin. Endocr Metab Immune drug discov 6: 18-23.