Hipercortisolismo cíclico por adenoma hipofisario
Sara Gómez R.1, Isabel Pavón de P.1, Naiara Modroño M.1, Carmen Pérez B.1 y Pablo Carrasco L.1
Cyclic hypercortisolism due to pituitary adenoma
1Servicio de Endocrinología y Nutrición del Hospital Universitario de Getafe, Madrid. España.
Conflicto de intereses:
Ninguno de los autores presenta conflicto de intereses.
Correspondencia:
Carretera de Toledo, Km 12,500, 28905 Getafe, Madrid
Teléfono: 916 83 93 60
sgomezr88@gmail.com
Recibido: 04-04-2017
Aceptado: 08-08-2017A case study of a 41 years old woman with cyclic hypercortisolism is explained. AT the beginning, its manegment was shrinking the tumor, however afterward she needs medical treatment during cycles. The fluctuating clinical and discrepant bioquemical findings make it hard to diagnose. A review of this rare disorder is explained.
Key words: Cyclic hypercortisolism; cyclic Cushing sindrome; pituitary adenoma.
Mujer de 41 años con IMC 24 kg/m2, que en un estudio por glucemia basal alterada e hipertensión arterial se detectó cifras compatibles con hipercortisolismo. En el interrogatorio dirigido refería alteraciones menstruales, hirsutismo, aumento de tejido adiposo a nivel abdominal y debilidad proximal en miembros inferiores. Presentaba cortisol libre urinario (CLU) 387 µg/24 h (4,30-176,00 µg/24 h); Cortisol tras 1 mg de dexametasona 16 mcg/dL; Cortisol nocturno 16,7 mcg/dL (< 1,8 mcg/dl) (Cortisol 8 h: 20,9 mcg/dl). Para el diagnóstico etiológico realizamos ACTH 158 pg/ml; Cortisol tras 8 mg de dexametasona 4,4 mcg/dl; Estimulación con Vasopresina con la que se constató una elevación de la ACTH de 150% y cortisol 50%. Todo ello orientaba a un origen hipofisario por lo que se realizó una resonancia magnética de hipófisis que mostraba una lesión hipointensa cercana al seno cavernoso izquierdo de 5 mm que podría corresponder a un adenoma hipofisario con mínima lateralización contralateral del tallo (Figura 1).
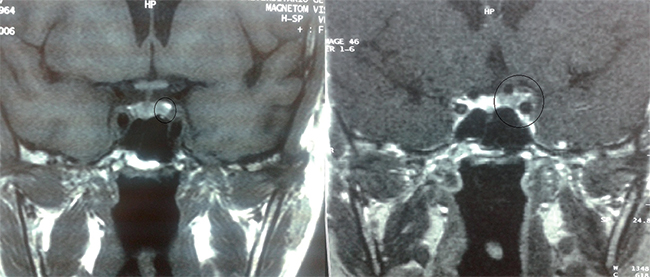
Con el diagnóstico altamente probable de Síndrome de Cushing ACTH dependiente de origen hipofisario, fue intervenida por vía transesfenoidal para resección del adenoma. El informe anatomopatológico de la muestra fue de adenoma hipofisario con inmunohistoquímica negativa para todas las hormonas. A pesar del resultado anatomo-patológico no concluyente con la sospecha clínica, la paciente presentó remisión clínica y analítica del hipercortisolismo durante 2 años. Tras suspender hidroaltesona pautado en la cirugía, presentaba cortisol basal: 10,5 mcg/dl, ACTH: 43 pg/ml, CLU: 76 µg/24 h.
Tras este período comenzó con un episodio superponible al anterior, en este momento presentaba cortisol basal 35 µg/dl; CLU 378 µg/24 h; ACTH de 113 pg/ml; Cortisol tras 1 mg dexametasona 2,23 mcg/dl; Cortisol tras 8 mg dexametasona: 1,69 mcg/dl. Se realizó un TC torácico-abdomino-pélvico y un Octreoscan para descartar un origen ectópico, todo ello normal. La resonancia magnética de hipófisis mostró una imagen de 3 mm hipointensa en lado izquierdo. Antes de realizar más estudios la paciente suspendió el ketoconazol que recibía tras el inicio del brote y presentó remisión espontánea del hipercortisolismo. Desde entonces ha presentado 2 nuevos episodios de hipercortisolismo de dos meses de duración y que han remitido espontáneamente (Figura 2). En uno de ellos se logró realizar un cateterismo de senos petrosos, confirmando el origen hipofisario del cuadro.
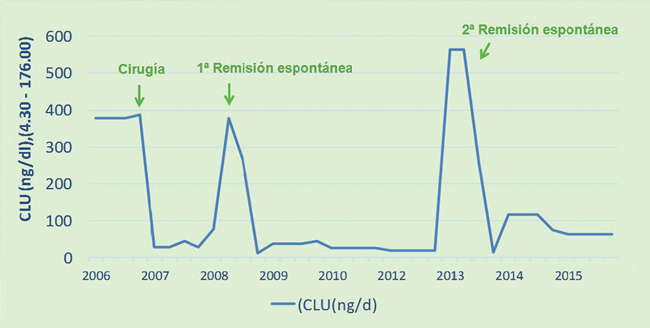
Figura 2. Evolución cronológica de la hormonogénesis cíclica expresados en CLU.
Por el curso clínico irregular que muestra podemos concluir que nos encontramos ante un caso de Síndrome de Cushing cíclico de origen hipofisario.
La definición clásica del Cushing cíclico consiste en presentar 3 picos de hipercortisolismo junto con 2 descensos. Es frecuente encontrar períodos de hipocortisolismo que requieren tratamiento corticoideo sustitutivo, que en nuestro caso no se han producido1.
Su prevalencia es mayor de lo que pudiera parecer a priori. Evaluando más estrechamente pacientes con síndrome de Cushing previamente a la realización de un tratamiento definitivo podemos hallar 17-36% de cursos cíclicos2.
Alexandraki et al3 y Meinardi et al2, recogen dos de las series más extensas de pacientes con hipercortisolismo cíclico (Tablas 1 y 2). Es importante destacar que la probabilidad de descubirir el adenoma y la curación es menor en el hipercortisolismo cíclico, lo cual traduce su dificultad en su manejo.
Tabla 1. Resumen de los casos expuestos en la revisión de Meinardi et al.
| Casos descritos en la literatura | Características clínicas de los 65 casos reportados en la literatura | |||
| Causas | Número de casos | Sexo femenino | 47 (72%) | |
| ACTH dependiente | 35 (54%) | Edad al diagnóstico (mediana, años) | 47 (0-72) | |
| Ectópico | 17 (26%) | Clínica S. Cushing | 61 (94%) | |
| Adrenal | 7 (11%) | Tiempo ciclos (mediana, días) | 212 (3-510) | |
| No clasificado | 6 (9%) | Tiempo interciclos (mediana, días) | 30 (1-2.160) | |
| Supervivencia | 94% (58/62) | |||
Adaptada de: Meinardi JR, Wolffenbuttel BHR, Dullaart RPF. 2007. Cyclic Cushing´s Syndorme: a clinical challenge. European Journal of Endocrinology
157: 245-254 (2).
Tabla 2. Resumen de los casos expuestos en la revisión de Alexandraki et al.
| Prevalencia de casos cíclicos | 30/201 (14,9%) |
| Sexo femenino | 26/30 (86%) |
| Casos en niños | 1/17 (5,58%) |
| Número de ciclos (mediana) | 2 (1-4) |
| Tiempo ciclos (mediana, años) | 3,8 ± 0,6 (0,2-26) |
| Tipo de ciclos | |
| Ciclos con clínica | 8 (14,8%) |
| Ciclos con clínica y bioquímica | 39 (72%) |
| Ciclos con bioquímica | 7 (13%) |
| Edad (media, años) | 42,3 ± 2 (17-72) |
| Presencia macroadenoma | 2 (6,67) |
| Adrenalectomía bilateral ) | 8 (26%) |
| Síndrome de Nelson | 2/8 (25%) |
| Terapia Block and replace | 2 (6,67%) |
| Neurocirugía | n = 19 |
| Curados | 6 (31%) |
| Recurrencia | 4 (21%) |
| No curados | 9 (47%) |
| Identificación adenoma en pieza quirúrgica | 9/19 (47%) |
La causa más frecuente es el adenoma hipofisario 54-80%, seguido del tumor productor de ACTH ectópico sobre todo los carcinoides. El origen adrenal supone un 10% aproximadamente2. En nuestro caso, la paciente presentaba un adenoma hipofisario con inmunohistoquímica negativa y, sin embargo, los resultados del cateterismo de senos petrosos resultaron ser diagnósticos de un origen hipofisario. Es posible que en el adenoma de nuestra paciente coexistan dos estirpes celulares: la primera de ellas, sin expresión hormonal que se extirpó; y la segunda ellas con sobreproducción hormonal cíclica, no extirpada.
Tiene una mayor afinidad por el sexo femenino (3:1) y la edad de presentación es normalmente 40-50 años. La duración de los ciclos de hipercortisolismo es muy variable, comprende un período de días a meses, sin embargo, en un mismo paciente suele ser constante; en nuestro caso 2 meses aproximadamente. Las fases intercíclicas suelen ser irregulares en un mismo individuo2.
Existen varias hipótesis que justifican el origen del cuadro, ninguna de ellas demostrada. La alternancia entre muerte y crecimiento celular en el contexto de una necrosis hemorrágica del tumor o un desequilibrio en las señales hipotalámicas son algunas de las teorías existentes2.
El diagnóstico del Cushing cíclico es un reto para el clínico y requieren un seguimiento estrecho en el tiempo. Las técnicas más recomendadas para la detección de los brotes son el CLU y el cortisol salivar4. La medición de cortisol en el pelo podría ser de utilidad en esta entidad ya que el análisis de los niveles se correlacionan adecuadamente con el tiempo de evolución, detectándose visiblemente los brotes. La limitación de esta técnica radica en la amplia variación en situaciones de estrés, obesidad, diabetes, etc.5,6. Otro método diagnóstico útil es el cociente cortisol/creatinina en la primera micción del día. Este ratio es altamente sensible a situaciones de hipercortisolismo, sin embargo, requiere una monitorización urinaria diaria7.
El tratamiento es el de la causa subyacente, en nuestro caso un adenoma hipofisario. Como particularidad se ha descrito la terapia “block and replace” que consiste en bloquear el sistema corticoadrenal y sustituir mediante tratamiento corticoideo; así evitamos las manifestaciones fluctuantes de los brotes, manteniendo constante el nivel corticoideo8.
Debemos sospechar esta entidad en casos con un hipercortisolismo clínico manifiesto y bioquímicamente negativo o viceversa. En estos casos se recomienda realizar un seguimiento estrecho con el fin de llegar al diagnóstico sindrómico.
Referencias bibliográficas
- Brown RD, Van Loon GR, Orth DN, et al. 1973. Cushing´s disease with periodic hormonogenesis: one explanation for paradoxical response to dexamethasone. JCEM 36: 445-51.
- Meinardi JR, Wolffenbuttel BHR, Dullaart RPF. 2007. Cyclic Cushing´s Syndorme: a clinical challenge. European Journal of Endocrinology 157: 245-54.
- Alexandraki KI, Kaltsas GA, Isidori AM, Akker SA, Drake WM, Chew SL, et al. 2009. The prevalence and characteristic features of cyclicity and variability in Cushing’s disease. European Journal of Endocrinology 160: 1011-8.
- Nieman LK, Biller BMK, Findling JW, et al. 2008. The Diagnosis of Cushing’s Syndrome: An Endocrine Society Clinical Practice Guideline. JCEM (5): 1526-40.
- Manenschijn L, Koper JW, van den Akker ELT, de Heide LJM, et al. 2012. A Novel Tool in the Diagnosis and Follow-Up of (Cyclic) Cushing’s Syndrome: Measurement of Long-Term Cortisol in Scalp Hair. JCEM 97 (10): E1836-E1843.
- Wester VL, van Rossum EFC. 2015. Clinical applications of cortisol measurement in hair. European Journal of Endocrinology 173 (4): M1-M10.
- Graham UM, Hunter SJ, McDonnell M, et al. 2013. A Comparison of the Use of Urinary Cortisol to Creatinine Ratios and Nocturnal Salivary Cortisol in the Evaluation of Cyclicity in Patients with Cushing’s Syndrome. JCEM 98 (1): E72-E76.
- Nieman LK, Biller BMK, Findling JW, et al. 2015. Treatment of Cushing Syndome: An Endocrine Society Practice Guideline. JCEM 100 (8): 2807-31.