Compromiso de seno cavernoso como presentación de cáncer anaplásico de tiroides
Francisca Gajardo1, Vjerocka Inostroza1, Pamela Invernizzi2, Cristóbal Campos2, Marcelo Mardones2, Félix Vásquez3, Nicolás Crisosto3, Cecilia Pereira3, Paola Hernández3, Erika Díaz3, Amanda Ladrón De Guevara3, Miguel Domínguez3, Jaime Morán3, Andrés Rodríguez4, Patricia Arroyo5 y G. Donoso6
Cavernous sinus involvement as presentation of anaplastic thyroid cancer
1Becada de Medicina Interna, Universidad de Chile, Hospital San Juan de Dios, Santiago, Chile.
2Servicio de Endocrinología, Hospital San Juan de Dios, Santiago, Chile.
3Cirugía cabeza y cuello, Hospital San Juan de Dios, Santiago, Chile.
4Anatomía patológica, Hospital San Juan de Dios, Santiago, Chile.
5Radiología, Hospital San Juan de Dios, Santiago, Chile.
6Medicina Nuclear, Hospital San Juan de Dios, Santiago, Chile.
Autores no declaran ningún conflicto de interés.
Correspondencia:
Felix Vásquez Rojas
Fono: 56-2-25742338
felix.vasquezr@yahoo.com
Recibido: 14-07-2017
Aceptado: 02-09-2017
Anaplastic thyroid cancer is an uncommon malignant tumor, usually fatal, primarily affecting older adults and doesn’t have effective systemic therapy. The median survival is less than 6 months from diagnosis. Brain metastases are low frequency and reach 18%. We present the case of a patient with papillary carcinoma of the thyroid who takes an aggressive form, becoming anaplastic carcinoma, with involvement of the central nervous system (CNS) manifested by paralysis of the cranial nerve IV, which is rare clinical condition.
Key words: Anaplastic thyroid cancer, Cavernous Sinus Thrombosis, Papillary thyroid cancer.
La hipofisitis es un cuadro caracterizado por la infiltración lifocítica de la glándula pituitaria. Dentro de su clasificación encontramos la infundibuloneurohipofisitis que afecta principalmente al tallo hipofisiario, infundíbulo y neurohipófisis. Su principal cuadro clínico es la diabetes insípida central, que lo diferencia habitualmente del compromiso global de la pituitaria o panhipofisitis. Tiene generalmente un curso crónico que puede ser adecuadamente manejado con desmopresina. A partir de un caso clínico presentamos el curso natural de esta enfermedad e ilustramos los cambios anatómicos clásicos en la región selar a través de la resonancia magnética.
Presentación del caso
Paciente de sexo femenino de 65 años de edad, con antecedentes de hipertensión arterial y obesidad mórbida. Historia de 2 años de evolucion de aumento progresivo de volumen cervical derecho. Ecotomografía tiroidea (realizada en octubre de 2014), describe lóbulo tiroideo derecho reemplazado por gran nódulo sólido, heterogéneo, sin calcificaciones y leve vascularización intralesional, sin adenopatías. No continúa estudio ni mantiene seguimiento.
En abril de 2016 consulta en servicio de urgencia por cuadro de diplopía y cefalea intensa. Se objetiva parálisis de VI par derecho e importante aumento de volumen cervical, de consistencia dura, asociada a eritema y lesión ulcerada a nivel supraclavicular derecho.
Se realiza angiotomografía craneal y cervical, que revela gran masa cervical derecha de origen tiroideo con realce heterogéneo de 95 x 67 x 82 mm, la cual compromete músculos esternocleidomastoideo y platisma, desplazando la tráquea (Figura 1). Adenopatías cervicales GI y GIIa de hasta 11 mm, trombosis del seno transverso, sigmoideo (Figura 2a) y vena yugular derecha. Lesiones líticas en región pretroclival de 17 mm que contacta región posterior de seno cavernoso y canal medular (Figura 2b). Tomografía de tórax: 5 nódulos pulmonares indeterminados de 3-4 mm, adenopatías cervicales inferiores, retrotraqueales y masa tiroidea previamente descrita que se extiende hacia tórax. Estudio tiroideo: TSH 4,47 ulU/ml; T4 Libre 1,24 ng/dl, anticuerpo antitiroglobulina 25 UD OMS y tiroglobulina 763 ug/L.
La biopsia de lesión bajo visión ecográfica concluye cáncer papilar. Ingresa a cirugía, describiéndose gran masa con invasión de músculo esternocleidomastoideo, tejido pretiroideo, vía aérea, arteria carótida y con extensión a tórax. Se realiza resección ampliada de masa tiroidea derecha, esternocleidomastoideo, nervio espinal y vena yugular interna derecha, además de traqueostomía. Se conserva lóbulo izquierdo por considerarse irresecable.
La biopsia concluye carcinoma papilar con desdiferenciación anaplásica (Figura 3), infiltrante en piel y tejidos blandos, con compromiso de márgenes quirúrgicos. Linfonodo de 12 mm con macrometástasis de carcinoma papilar.
En comité se plantea continuar tratamiento con radioterapia, sin embargo, la paciente evoluciona tórpidamente, falleciendo al mes post diagnóstico.
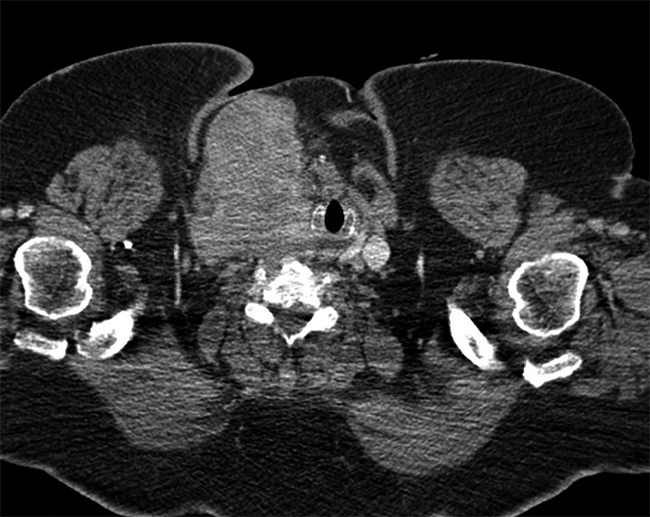
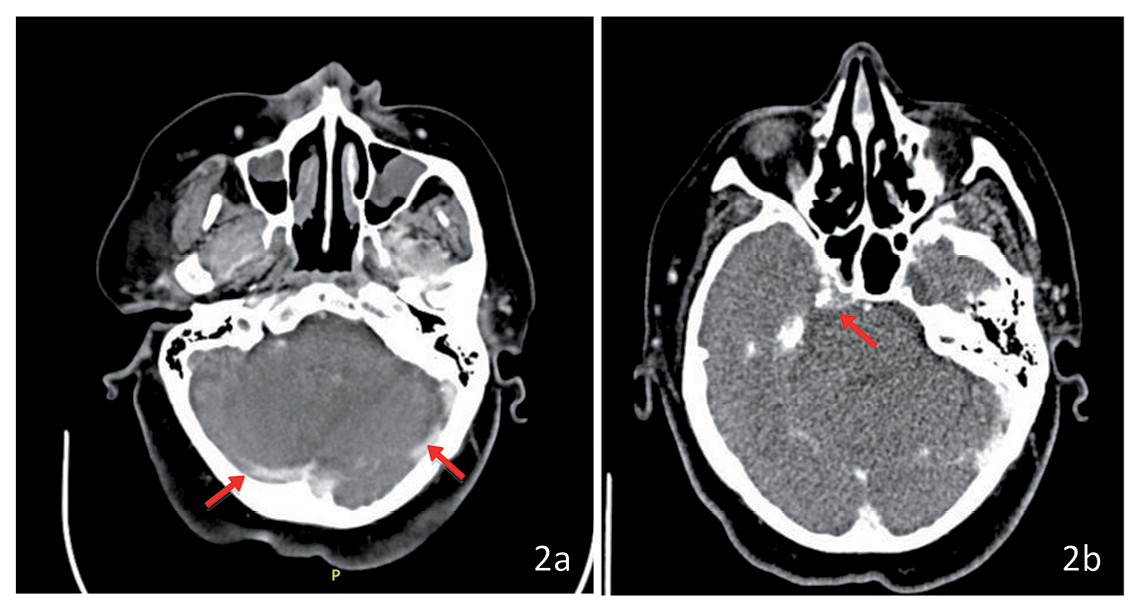 Figura 2. Corte axial de TAC de encéfalo; a: Trombosis del seno transverso y sigmoideo (indicado mediante flechas rojas); b: Compromiso osteolítico de región petroclival (indicado con flecha roja).
Figura 2. Corte axial de TAC de encéfalo; a: Trombosis del seno transverso y sigmoideo (indicado mediante flechas rojas); b: Compromiso osteolítico de región petroclival (indicado con flecha roja).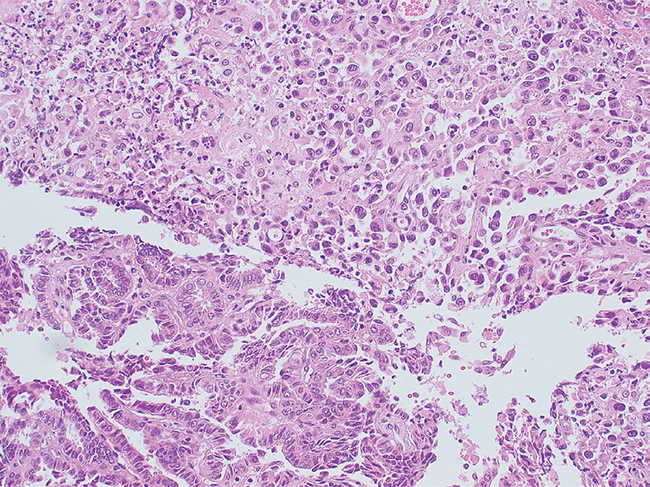 Figura 3. Corte histológico con zonas correspondientes a cáncer anaplásico de tiroides y carcinoma papilar de tiroides en la misma muestra.
Figura 3. Corte histológico con zonas correspondientes a cáncer anaplásico de tiroides y carcinoma papilar de tiroides en la misma muestra.Discusión
El cáncer papilar es el carcinoma de tiroides más común, con pronóstico favorable y sobrevida en etapa 1 de aproximadamente 100%1. La transformación a anaplásico es poco frecuente2,3. Kitamura et al.15 describe una serie retrospectiva de 161 pacientes fallecidos por carcinoma de tiroides, de los cuales 99 tenían cáncer anaplásico. De estos, sólo 2/3 contaban con el diagnóstico anatomopatológico previo y aproximadamente la mitad de los pacientes tienen historia de haber presentado un cáncer bien diferenciado de tiroides, ya sea folicular o papilar.
La incidencia del cáncer anaplásico de tiroides ha disminuido de un 16% a un 8% durante los ultimos años debido a un aumento en la detección precoz del cáncer papilar y folicular2,3. La incidencia mundial anual descrita es de 1-2 casos por 1.000.000 habitantes4 y representa solo el 2 a 5% de todos los carcinomas de tiroides5. La sobrevida media es de 3 a 6 meses desde el momento del diagnóstico, con tasa de supervivencia al año de 10 al 20%2,5. Afecta principalmente a mujeres entre la sexta y séptima décadas de la vida, correspondiendo éstas al 55 a 75% de los casos5,6. El tamaño del tumor generalmente varía de 6 a 9 cm2. En nuestro centro, observamos una incidencia de 9,9%, con una letalidad del 100% a los 2 meses, sin lograr demostrar efectividad a los tratamientos otorgados.
Es el más agresivo de los carcinomas de tiroides, invadiendo rápidamente estructuras adyacentes. Aproximadamente un 50% de los casos tiene metástasis a distancia y solo un 10% está confinado solo a la glándula tiroides5-7.
Las metastasis del sistema nervioso central son comunes en los pacientes con cáncer, ocurren entre un 20-30%8. A pesar de ello, las metástasis cerebrales derivadas del cáncer de tiroides son muy raras, solo ocurren en aproximadamente 0,9-1,5% de todos los cánceres diferenciados de tiroides y un 4,5-18% de todos los cánceres con otras metástasis a distancia9. El pronóstico de estos pacientes es malo y tienen baja sobrevida en relación a los pacientes que no la presentan.
Besic et al.10 describe en autopsias los sitios más frecuentes de metástasis a distancias del cáncer anaplásico de tiroides: pulmón (78%), ganglios linfáticos intratorácicos (58%), ganglios linfáticos cervicales (51%), pleura (29%), glándulas suprarrenales (24%), hígado (20%), cerebro (18%) y ganglios linfáticos retroperitoneales (18%).Giuffrida et al.4 describe, además, metástasis en sitios mucho menos comunes, por ejemplo en corazón.
La terapia multimodal combinando cirugía, quimioterapia y radioterapia, podría lograr mejores resultados en la supervivencia de algunos pacientes; sin embargo, el cáncer anaplásico de tiroides tiene una tasa de curación muy baja, incluso con los tratamientos extremadamente radicales 2,4.
Actualmente, la resección quirúrgica y los tratamientos adyuvantes de las metástasis intracraneales en casos de carcinomas de tiroides, parecen resultar en una mejor supervivencia en comparación con lo reportado en estudios pasados. Considerando el curso grave de las metástasis intracraneales, la detección precoz y el tratamiento agresivo de los pacientes con buen performance status, son cruciales para obtener buen rendimiento11,12.
Actualmente, no hay enfoques terapéuticos verdaderamente eficaces para el cáncer anaplásico de tiroides que puedan mejorar la supervivencia de estos pacientes. Hasta la fecha no hay estudios publicados que cuenten con estándares de alta calidad para caracterizar la clínica, el comportamiento y los resultados de estos pacientes13.
Este caso recalca la importancia en la detección y tratamiento precoz del carcinoma de tiroides, evitando la posible transformación a anaplásico. Una vez frente a este tipo de desdiferenciación, debe descartarse dirigidamente la existencia de lesiones secundarias a nivel del SNC y tener presente las posibles manifestaciones clínicas secundarias a estas.
Referencias bibliográficas
- American Cancer Society, Thyroid Cancer, 2016.
- Are C, Shaha AR. 2006. Anaplastic thyroid carcinoma: biology, pathogenesis, prognostic factors, and treatment approaches. Ann Surg Oncol 13: 453-464.
- Albores-Saavedra J, Henson DE, Glazer E, Schwartz AM. 2007. Changing patterns in the incidence and survival of thyroid cancer with follicular phenotype-papillary, follicular, and anaplastic: a morphological and epidemiological study. Endocr Pathol 18: 1-7.
- Giuffrida D, Gharib H. 2000. Anaplastic thyroid carcinoma: current diagnosis and treatment. Ann Oncol 11: 1083-1089.
- Ragazzi M, Ciarrocchi A, Sancisi V, Gandolfi G, Bisagni A,
Piana S. 2014. Update on anaplastic thyroid carcinoma: morphological, molecular, and genetic features of the most aggressive thyroid cancer. International Journal of Endocrinology, Article ID 790834, 13 pages. - Chiacchio S, Lorenzoni A, Boni G, Rubello D, Elisei R,
Mariani G. 2008. Anaplastic thyroid cancer: prevalence, diagnosis and treatment. Minerva Endocrinol 33: 341-357. - Nagaiah G, Hossain A, Mooney CJ, Parmentier J, Remick SC. 2011. Anaplastic thyroid cancer: a review of epidemiology, pathogenesis, and treatment. J Oncol 2011: 542358.
- Sul J, Posner JB. 2007. Brain metastases: epidemiology and pathophysiology. Cancer Treat Res 136: 1-21.
- Dinneen SF, Valimaki MJ, Bergstralh EJ, Goellner JR, Gorman CA, Hay ID. 1995. Distant metastases in papillary thyroid carcinoma: 100 cases observed at one institution during 5 decades. J Clin Endocrinol Metab 80 (7): 2041-2045.
- Besic N, Gazic B. 2013. Sites of metastases of anaplastic thyroid carcinoma: autopsy findings in 45 cases from a single institution. Thyroid 23 (6): 709-713.
- Chiu AC, Delpassand ES, Sherman SI. 1997. Prognosis and treatment of brain metastases in thyroid carcinoma. J Clin Endocrinol Metab 82 (11): 3637-42.
- Heui Seung Lee, Heon Yoo, Seung Hoon Lee, Ho Shin Gwak, Sang Hoon Shin. Clinical characteristics and follow-up of intracranial metastases from thyroid cáncer, Acta Neurochir DOI 10.1007/s00701-015-2611-5.
- Glaser SM, Mandish SF, Gill BS, Balasubramani GK, Clump DA, Beriwal S. 2016. Anaplastic thyroid cancer: Prognostic factors, patterns of care, and overall survival. Head Neck 38 Suppl 1: E2083-90.
- Ryan L. Neff RL, Farrar WB, Kloos RT, Burman KD. 2008. Anaplastic thyroid cancer. Endocrinology Metabolism Clinics of North America 37: 525-538.
- Kitamura Y, Shimizu K, Nagahama M, et al. 1999. Immediate causes of death in thyroid carcinoma: clinicopathological analysis of 161 fatal cases. J Clin Endocrinol Metab 84: 4043-4049.